Perbedaan antara emisi dan spektrum penyerapan
- 2803
- 831
- Rodney Hegmann

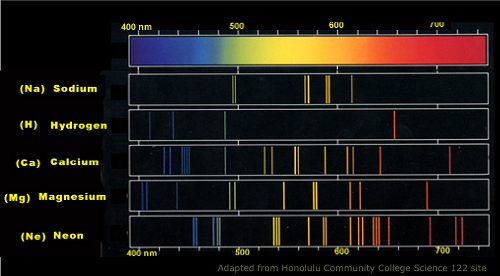
Spektrum emisi atom natrium
Emisi vs. Spektrum serapan
Seorang ahli kimia yang bertujuan untuk menemukan komposisi unsur zat atau larutan tertentu dapat membedakan atom melalui emisi dan/atau spektroskopi penyerapan. Kedua proses diarahkan untuk pengamatan elektron dan foton saat mengalami cahaya. Spektrofotometer bersama dengan sumber cahaya kemudian diperlukan dalam proses ini. Ilmuwan perlu memiliki daftar nilai untuk kedua emisi penyerapan untuk setiap atom sebelum membuat zat tersebut menjadi spektroskopi.
Misalnya, ketika ilmuwan menemukan sampel dari area yang jauh dan bertujuan untuk mempelajari komposisi masalah tersebut, ia dapat memilih untuk membuat sampel menjadi emisi atau spektroskopi penyerapan. Dalam spektrum serapan, ia seharusnya mengamati bagaimana elektron atom menyerap energi elektromagnetik dari sumber cahaya. Ketika cahaya diarahkan ke atom, ion, atau molekul, partikel cenderung menyerap panjang gelombang yang dapat menggairahkannya dan menyebabkan mereka berpindah dari satu kuantum ke kuantum lainnya. Spektrofotometer dapat mencatat jumlah panjang gelombang yang diserap, dan ilmuwan kemudian dapat merujuk pada daftar karakteristik elemen untuk menentukan komposisi sampel yang dikumpulkan.
Spektrum emisi dilakukan dengan proses penundukan cahaya yang sama. Namun, dalam proses ini, ilmuwan mengamati jumlah cahaya atau energi panas yang dipancarkan oleh foton atom yang membuat mereka kembali ke kuantum aslinya.
Pikirkan seperti ini: Matahari adalah pusat atom, yang terdiri dari foton dan neutron. Planet yang mengorbit matahari adalah elektron. Ketika senter raksasa diarahkan ke bumi (sebagai elektron), bumi menjadi bersemangat dan bergerak ke orbit Neptunus. Energi yang diserap oleh bumi dicatat dalam spektrum penyerapan.
Saat senter raksasa dilepas, bumi kemudian memancarkan cahaya agar dapat kembali ke keadaan aslinya. Dalam kasus seperti itu, spektrofotometer mencatat jumlah panjang gelombang yang dipancarkan oleh Bumi agar ilmuwan menentukan jenis elemen yang terdiri dari tata surya.
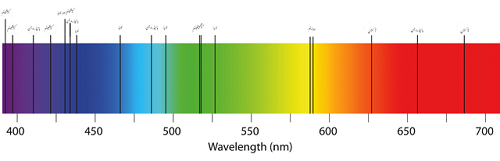
Spektrum serapan dari beberapa elemen
Selain itu, penyerapan tidak memerlukan eksitasi ion atau atom, tidak seperti spektrum emisi. Keduanya perlu memiliki sumber cahaya, tetapi ini harus bervariasi dalam dua proses. Lampu kuarsa biasanya digunakan dalam penyerapan, sementara pembakar cocok untuk spektrum emisi.
Perbedaan lain antara dua spektrum terletak pada output "cetak". Dalam mengembangkan gambar, misalnya, spektrum emisi adalah foto berwarna, sedangkan spektrum penyerapan adalah cetakan negatif. Inilah sebabnya: Spektrum emisi dapat memancarkan cahaya yang memanjang ke berbagai rentang spektrum elektromagnetik, sehingga menghasilkan garis berwarna dengan gelombang radio berenergi rendah ke sinar gamma berenergi lebih tinggi. Warna dalam prisma biasanya diamati dalam spektrum ini.
Di sisi lain, penyerapan dapat memancarkan beberapa warna ditambah dengan garis kosong. Ini karena atom menyerap cahaya pada frekuensi yang bergantung pada jenis elemen yang ada dalam sampel. Cahaya yang dipanaskan kembali dalam proses tidak mungkin dipancarkan ke arah yang sama dengan foton yang diserap berasal dari. Karena cahaya dari atom tidak dapat diarahkan ke ilmuwan, lampu tampaknya memiliki garis hitam karena gelombang yang hilang dalam spektrum elektromagnetik.
Ringkasan:
1.Spektrum emisi dan penyerapan keduanya dapat digunakan dalam menentukan komposisi materi.
2.Keduanya menggunakan sumber cahaya dan spektrofotometer.
3.Spektrum emisi mengukur panjang gelombang cahaya yang dipancarkan setelah atom tereksitasi dengan panas, sedangkan penyerapan mengukur panjang gelombang yang diserap oleh atom.
4.Spektrum emisi memancarkan semua warna dalam spektrum elektromagnetik, sedangkan penyerapan dapat memiliki beberapa warna yang hilang karena pengalihan kembali emisi foton yang diserap.
- « Perbedaan antara keterampilan motorik kotor dan halus
- Perbedaan antara epidemiologi dan etiologi »

