Senyawa vs. Campuran

- 1799
- 501
- Homer Hartmann
Senyawa adalah zat murni. Mereka terbuat dari jenis molekul yang sama. Setiap molekul suatu senyawa terbuat dari dua atau lebih jenis atom yang terikat secara kimia. Campuran terbuat dari dua atau lebih zat - elemen atau senyawa - yang dicampur secara fisik tetapi tidak secara kimia; mereka tidak mengandung ikatan atom.
Grafik perbandingan
| Menggabungkan | Campuran | |
|---|---|---|
| Definisi | Senyawa mengandung atom dari berbagai elemen yang secara kimia digabungkan bersama dalam rasio tetap. | Campuran adalah kombinasi dari dua zat atau lebih di mana tidak ada kombinasi atau reaksi kimia. |
| Komposisi | Senyawa mengandung elemen yang berbeda dalam rasio tetap yang disusun dengan cara yang ditentukan melalui ikatan kimia. Mereka hanya mengandung satu jenis molekul. Elemen yang menyusun senyawa digabungkan secara kimia. | Campuran mengandung berbagai elemen dan senyawa tetapi rasionya tidak diperbaiki juga tidak dikombinasikan melalui ikatan kimia. Bahan -bahannya dicampur secara fisik tetapi terpisah secara kimia. Seringkali mereka tampak berbeda. |
| Kemampuan untuk mogok | Senyawa dapat dipisahkan menjadi zat yang lebih sederhana dengan metode/reaksi kimia. | Campuran dapat dipisahkan menjadi zat yang lebih sederhana dengan metode fisik atau mekanis. |
| Contoh | Air (H2O), natrium klorida (NaCl), natrium bikarbonat (NAHCO3) dan asam klorida (HCl) adalah contoh senyawa. | Garam dalam air; pasta dan saus; pasir; kerikil; solusi seperti menggosok alkohol, amalgam gigi, uap di udara; koloid seperti mayones, susu, keju; suspensi kasar seperti lumpur dalam air, minyak dalam air. |
| Perwakilan | Senyawa diwakili menggunakan rumus kimianya yang mewakili simbol elemen konstituennya dan jumlah atom dari setiap elemen dalam satu molekul senyawa. | Campuran tidak dapat diwakili oleh formula kimia. |
| Sifat kimia dan fisik | Senyawa memiliki sifat kimia dan fisik spesifik yang berbeda dari unsur -unsur konstituennya karena unsur -unsur konstituen kehilangan sifatnya ketika mereka bergabung untuk membuat senyawa. | Campuran tidak memiliki sifat kimia dan fisik yang spesifik dan konsisten. Mereka mencerminkan sifat -sifat zat penyusunnya, yang mempertahankan sifat aslinya. e.G. Susu cokelat mempertahankan sifat cokelat dan susu |
| Tipe | Jumlah senyawa kimia yang besar, hampir tidak terbatas. Senyawa diklasifikasikan ke dalam senyawa molekul, senyawa ionik, senyawa intermetalik dan kompleks. | Padatan, cairan, dan gas dapat digabungkan untuk membuat campuran. Campuran bisa homogen atau tidak homogen. |
| Rasio massa | Senyawa memiliki rasio massa spesifik. e.G. Pirit memiliki 46.6% besi dan 53.4% belerang berdasarkan massa. Ini berlaku untuk semua pirit tidak peduli ukuran sampel. | Campuran memiliki rasio massa variabel tergantung pada jumlah bahan yang telah digabungkan dalam campuran. |
Konstituen senyawa dan campuran
Senyawa terdiri dari unsur -unsur, yang merupakan zat murni dengan hanya satu jenis atom. Atom -atom elemen membentuk ikatan untuk menggabungkan dan membentuk molekul senyawa. Senyawa ini mengandung distribusi yang seragam dari molekul -molekul ini.
Senyawa memiliki karakteristik fisik dan kimia yang berbeda dari elemen komponennya. Tidak mungkin untuk melihat elemen saat Anda melihat senyawa. e.G. Air terbuat dari hidrogen dan oksigen tetapi Anda tidak dapat melihat salah satu elemen secara terpisah saat Anda melihat air. Garam terbuat dari natrium dan klorida tetapi sifat fisik dan kimia garam benar -benar berbeda dari natrium atau klorida.
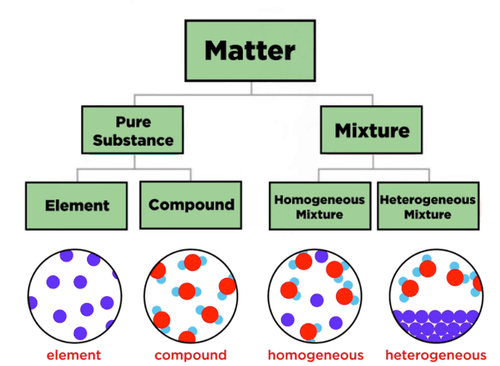 Jenis materi: elemen, senyawa, campuran homogen dan heterogen.
Jenis materi: elemen, senyawa, campuran homogen dan heterogen. Baik elemen dan senyawa disebut zat murni karena hanya mengandung satu jenis molekul. Campuran mengandung dua atau lebih jenis zat murni. Molekul zat ini tidak membentuk ikatan kimia apa pun dalam campuran. Komponen campuran mempertahankan kemandirian kimianya tetapi secara fisik berbaur satu sama lain. Seringkali mungkin untuk melihat komponen -komponen ini dan membedakannya secara visual.
Memisahkan komponen
Elemen komponen suatu senyawa hanya dapat dipisahkan melalui reaksi kimia yang merusak ikatan atom yang mengikat molekulnya.
Bahan -bahan campuran dapat dipisahkan dengan cara fisik seperti sedimentasi atau dekantasi.

