Perbedaan antara kristal dan amorf

- 2258
- 468
- Richard Hegmann MD
Amorf dan kristal adalah dua keadaan yang menggambarkan padatan khas dalam kimia. Menggunakan eksperimen difraksi sinar-X, struktur padatan dapat dikategorikan menjadi kristal atau amorf (non-kristal).
Padatan adalah di antara tiga keadaan dasar materi yang mencakup cairan dan gas. Mereka ditandai dengan struktur molekul, ion dan atom yang kaku yang disusun dengan cara yang tertib atau tidak tertib. Pengaturan tertib atau tidak tertib ini telah menyebabkan kategorisasi sebagai amorf dan kristal dan artikel ini mengungkap perbedaan utama antara kedua istilah tersebut.

Apa itu kristal?
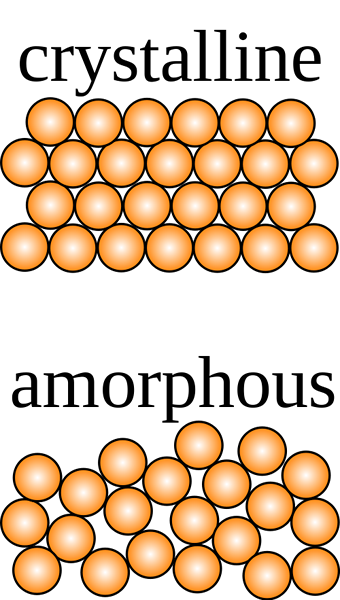
Padatan kristal adalah bahwa di mana partikel-partikel konstituen diatur secara tertib dalam pola tiga dimensi yang disebut kisi kristal dengan gaya intermolekul yang seragam, dan partikel berpotongan pada sudut karakteristik kristal.
Struktur internal memiliki bentuk geometris yang berbeda, dan menunjukkan pembelahan yang jelas saat dipotong di mana saja dalam struktur. Pola tiga dimensi yang terlihat menggunakan sinar-X digunakan untuk mengidentifikasi padatan. Namun, tidak mudah untuk mendeteksi perbedaan antara padatan kristal dan non-kristal dengan menyentuhnya. Mereka berbeda satu sama lain dalam banyak aspek termasuk sifat kimia dan fisik.
Padatan kristal (kristal) membutuhkan suhu ekstrem untuk memecahkan gaya antarmolekul. Mereka memiliki panas yang pasti dari fusi dan titik leleh karena pengaturan seragam komponen mereka. Lingkungan setempat juga seragam. Namun, saat dipotong ke segala arah, sifat fisiknya berbeda sehingga dikenal sebagai anisotropik. Saat diputar di sekitar sumbu, struktur kristal tetap sama dan yang disebut sebagai susunan simetris molekul, atom atau ion.
Beberapa padatan kristal dapat berakhir menjadi amorf tergantung pada proses pendinginan. Yang lain mungkin memiliki komponen mereka tidak selaras karena adanya kotoran. Juga, zat pendingin dengan cepat dapat menyebabkan struktur amorf dengan bentuk geometris yang tidak teratur. Kuarsa, misalnya, adalah kristal dengan atom silikon dan oksigen secara tertib. Tapi, saat didinginkan dengan cepat, itu dapat menyebabkan kaca struktur amorf. Biasanya terjadi bahwa proses kristalisasi dihindari oleh zat peleburan dengan cepat untuk menghasilkan padatan amorf karena aplikasi industri yang luas. Karet, polimer, dan kaca adalah salah satu contoh sempurna dari padatan amorf penting yang sebagian besar digunakan untuk manfaatnya yang luar biasa dan sifat isotropik yang unik.
Indeks bias, kekuatan mekanik, konduktivitas termal dan konduktivitas listrik dari padatan kristal berbeda dalam arah yang berbeda. Itulah kelemahan dari jenis padatan ini dibandingkan dengan padatan non-kristal. Sisi baik dari padatan anisotropik adalah ia menunjukkan struktur internal yang diatur dengan sempurna dengan kekuatan atraksi yang seragam dalam kisi kristal. Itu menggambarkan sifat sebenarnya dari padatan dengan urutan jarak jauh dan struktur yang kaku.
Apa amorf?
Kata amorf berasal dari kata Yunani amorf yang berarti "tidak berbentuk". Ini adalah susunan partikel konstituen yang tidak berbentuk, tidak teratur, dan tidak teratur. Kekuatan antar-molekulnya tidak sama, juga jarak antara partikel. Saat membelah, padatan amorf menghasilkan fragmen atau permukaan melengkung karena bentuk geometris yang tidak teratur.
Beberapa padatan amorf dapat memiliki bagian dari pola yang diatur secara tertib yang disebut kristalit. Atom, ion atau molekul padatan tergantung pada proses pendinginan. Seperti yang disebutkan di atas, kristal kuarsa berbeda dengan kaca kuarsa karena proses kristalisasi. Tetapi, umumnya, banyak padatan amorf memiliki pola yang tidak teratur. Mereka biasanya disebut padatan super didinginkan karena struktur berbagi beberapa sifat dengan cairan. Juga, mereka tidak menunjukkan sifat sebenarnya dari padatan, tetapi masih sebagian besar digunakan dalam berbagai aplikasi.
Konduktivitas termal, kekuatan mekanik, konduktivitas listrik dan indeks bias adalah sama di semua arah padatan amorf. Ini menjelaskan dari mana nama isotropik berasal. Padatan tidak memiliki titik leleh yang tajam atau panasnya fusi yang pasti. Berbagai macam suhu perlu diterapkan sebelum mereka dapat meleleh karena tidak adanya serangkaian komponen yang dipesan. Selanjutnya, padatan amorf ditandai dengan urutan jarak pendek. Contoh padatan amorf termasuk polimer, karet, plastik dan kaca.
Jika padatan amorf dibiarkan lama di bawah titik lelehnya, ia dapat berubah menjadi padatan kristal. Itu dapat menggambarkan sifat yang sama yang dimiliki oleh padatan kristal.
Perbedaan utama antara amorf dan kristal
Struktur kristal dan amorf
Padatan kristal memiliki bentuk yang pasti dengan ion, molekul atau atom yang tertib. Jika dipotong, mereka menggambarkan pembelahan yang jelas dengan permukaan yang berpotongan pada sudut yang merupakan karakteristik kristal. Padatan amorf, di sisi lain, memiliki serangkaian komponen yang tidak teratur yang tidak menunjukkan bentuk yang pasti. Saat dipotong, mereka menunjukkan bentuk yang tidak teratur biasanya dengan permukaan melengkung. Komponen kristal disatukan oleh kekuatan antarmolekul yang seragam sedangkan pada padatan amorf gaya ini berbeda dari satu atom ke yang lain.
Titik peleburan kristal dan amorf
Padatan amorf tidak memiliki titik lebur yang pasti tetapi meleleh pada kisaran suhu yang luas karena bentuk yang tidak teratur. Padatan kristal, di sisi lain, memiliki titik leleh yang tajam.
Sifat fisik kristal dan amorf
Padatan kristal memiliki konduktivitas listrik yang berbeda, konduktivitas termal, indeks bias dan kekuatan mekanik dalam kristal dalam arah yang berbeda sehingga mereka disebut anisotropik. Amorf disebut isotropik karena sifat fisik yang sama dari kedua arah.
Contoh kristal dan amorf
Contoh padatan kristal termasuk NaCl, gula dan berlian sedangkan contoh padatan amorf termasuk kaca, karet dan polimer.
Lihat bagan perbandingan untuk ayat -ayat kristal amorf di bawah ini:
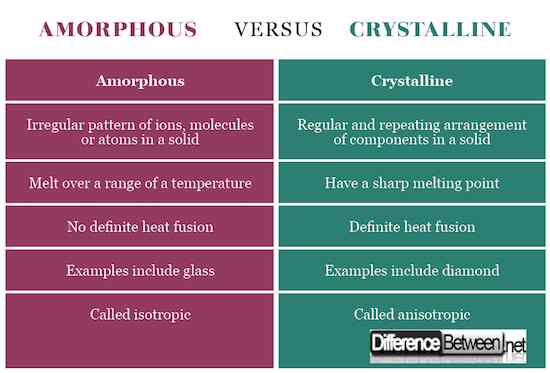
Ringkasan ayat -ayat kristal amorf
- Padatan kristal memiliki pola ion, atom atau molekul tiga dimensi reguler sedangkan padatan amorf memiliki pengaturan acak dari komponen-komponen ini
- Padatan kristal memiliki titik leleh yang tepat sedangkan padatan amorf meleleh pada kisaran suhu
- Padatan amorf menghasilkan fragmen dengan pola tidak teratur saat dibelah sedangkan padatan kristal menggambarkan bentuk yang pasti
- Kristal yang disebut anisotropik karena sifat fisik yang berbeda di semua arah sedangkan amorf disebut isotropik
- Contoh amorf termasuk kaca dan kristal termasuk berlian.

