Vs homogen. Campuran heterogen

- 858
- 52
- Mr. Doug Effertz
Campuran berbeda dari zat murni seperti elemen dan senyawa karena campuran mengandung zat yang berbeda yang digabungkan secara fisik tetapi tidak secara kimiawi. Komponen individu dalam campuran mempertahankan identitas mereka.
Campuran terdiri dari dua jenis: homogen dan heterogen. Campuran homogen memiliki komposisi dan penampilan yang seragam. Zat individu yang merupakan campuran homogen tidak dapat dibedakan secara visual. Di sisi lain, campuran heterogen terdiri dari dua atau lebih zat yang dapat diamati dengan jelas, dan bahkan dipisahkan secara relatif mudah.
Grafik perbandingan
Perbedaan - Persamaan -| Heterogen | Homogen | |
|---|---|---|
| Seragam | TIDAK | Ya |
| Anda dapat melihat bagian -bagiannya | Ya | TIDAK |
| Dapat dipisahkan secara fisik | Ya | TIDAK |
| Contoh | Salad, campuran jejak | Minyak zaitun, baja, garam dalam air |
| Terikat secara kimia | TIDAK | TIDAK |
Karakter fisik
Semua campuran terdiri dari dua atau lebih zat murni (elemen atau senyawa). Perbedaan antara campuran dan senyawa adalah bagaimana elemen atau zat bergabung untuk membentuknya. Senyawa adalah zat murni karena hanya mengandung satu jenis molekul. Molekul terbuat dari atom yang terikat bersama. Tetapi dalam campuran, elemen dan senyawa keduanya ditemukan bercampur secara fisik tapi tidak secara kimiawi-Tidak ada ikatan atom yang terbentuk antara zat murni yang merupakan campuran.
Tetapi terlepas dari ikatan atom, campuran bisa menjadi cukup kohesif. Biasa dipanggil solusi, Campuran yang homogen adalah zat -zat yang sangat baik sehingga tidak dapat dilihat secara individual dalam bentuk yang berbeda dan berbeda. Komposisi mereka seragam i.e., Sama di seluruh campuran. Keseragaman ini adalah karena konstituen campuran homogen terjadi dalam proporsi yang sama di setiap bagian campuran.
Sebaliknya campuran heterogen adalah salah satu di mana zat penyusun tidak terdistribusi secara seragam. Mereka sering dapat diceritakan secara visual dan bahkan dipisahkan secara relatif mudah, meskipun banyak metode yang ada untuk memisahkan solusi homogen juga.
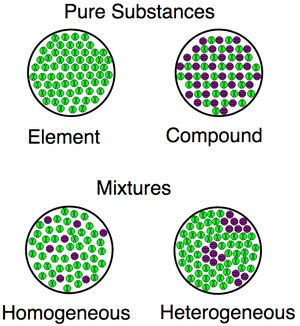 Visualisasi untuk perbedaan antara zat (senyawa, elemen) dan campuran (keduanya homogen dan heterogen).
Visualisasi untuk perbedaan antara zat (senyawa, elemen) dan campuran (keduanya homogen dan heterogen). Contoh campuran homogen dan heterogen
Contoh campuran heterogen adalah es batu (sebelum mereka meleleh) dalam soda, sereal dalam susu, berbagai topping di atas pizza, topping dalam yogurt beku, sekotak bermacam -macam kacang bermacam -macam. Bahkan campuran minyak dan air heterogen karena kepadatan air dan minyak berbeda, yang mencegah distribusi seragam dalam campuran.
Contoh campuran homogen adalah milkshake, jus sayuran campuran, gula dilarutkan dalam kopi, alkohol dalam air, dan paduan seperti baja. Bahkan udara yang ada di atmosfer kita adalah campuran homogen dari berbagai gas dan tergantung pada kota yang Anda hidup dalam polutan. Banyak zat, seperti garam dan gula, larut dalam air untuk membentuk campuran homogen.
Jenis campuran
Ada tiga keluarga campuran: solusi, suspensi dan koloid. Solusi homogen sementara suspensi dan koloid heterogen.
Larutan
Solusi adalah campuran homogen yang mengandung zat terlarut yang dilarutkan dalam pelarut, e.G. garam larut dalam air. Saat pelarut adalah air, itu disebut larutan berair. Rasio massa zat terlarut terhadap pelarut disebut konsentrasi larutan.
Solusi bisa likuid, gas atau bahkan padat. Tidak hanya itu, komponen individu dari solusi dapat berupa keadaan materi yang berbeda. Zat terlarut mengasumsikan fase (padat, cair atau gas) dari pelarut ketika pelarut adalah fraksi yang lebih besar dari campuran.
- Solusi gas: Saat pelarut adalah gas, hanya mungkin untuk melarutkan zat terlarut gas di dalamnya. Contoh paling umum dari solusi gas adalah udara di atmosfer kita, yaitu nitrogen (pelarut) dan memiliki zat terlarut seperti oksigen dan gas lainnya.
- Solusi Cair: Pelarut cair mampu melarutkan jenis zat terlarut apa pun.
- Gas dalam cairan: Contohnya termasuk oksigen dalam air, atau karbon dioksida dalam air.
- Cairan dalam cairan: Contohnya termasuk minuman beralkohol; Mereka adalah solusi etanol dalam air.
- Padatan dalam cairan: Gula atau larutan garam dalam air adalah contoh campuran tersebut. Banyak padatan dalam campuran cair tidak homogen sehingga mereka bukan solusi. Mereka bisa menjadi koloid atau suspensi.
- Solusi Solid: Pelarut Padat juga dapat melarutkan zat terlarut dari keadaan apa pun.
- Gas dalam padatan: Contohnya adalah hidrogen yang dilarutkan dalam paladium
- Cairan dalam padatan: Contohnya termasuk merkuri dalam emas, membentuk amalgam, dan air (kelembaban) dalam garam
- Solid dalam padat: paduan seperti baja, kuningan atau perunggu adalah contoh campuran seperti itu.
Penangguhan
Suspensi adalah campuran heterogen yang mengandung partikel padat yang cukup besar untuk sedimentasi. Partikel padat tidak larut dalam pelarut tetapi ditangguhkan dan mengambang bebas. Mereka lebih besar dari 1 mikrometer dan biasanya cukup besar untuk terlihat oleh mata telanjang. Contohnya adalah pasir dalam air. Fitur utama suspensi adalah bahwa partikel tersuspensi menetap dari waktu ke waktu jika dibiarkan tidak terganggu.
Koloid
Koloid heterogen seperti suspensi tetapi secara visual tampak homogen karena partikel-partikel dalam campuran sangat kecil-1 nanometer hingga 1 mikrometer. Perbedaan antara koloid dan suspensi adalah bahwa partikel -partikel dalam koloid lebih kecil dan partikel tidak akan mengendap dari waktu ke waktu.
| Larutan | Koloid | Penangguhan | |
|---|---|---|---|
| Homogenitas | Homogen | Heterogen pada tingkat mikroskopis tetapi homogen secara visual | Heterogen |
| Ukuran partikel | < 1 nanometer (nm) | 1 nm - 1 mikrometer (μm) | > 1 μm |
| Stabil secara fisik | Ya | Ya | Perlu menstabilkan agen |
| Menunjukkan efek Tyndall | TIDAK | Ya | Ya |
| Terpisah dengan centrifuge | TIDAK | Ya | Ya |
| Terpisah dengan dekantasi | TIDAK | TIDAK | Ya |
Teknis
Sampai batas tertentu, Anda dapat mengatakan (jika Anda bersikap pedantic) bahwa pertanyaan apakah campuran itu homogen atau heterogen tergantung pada skala di mana campuran sedang disampel.
Jika skala pengambilan sampel baik (kecil), itu bisa sekecil molekul tunggal. Dalam hal ini, sampel apa pun akan menjadi heterogen karena dapat digambarkan dengan jelas pada skala itu. Demikian pula, jika sampel adalah seluruh campuran, Anda bisa menganggapnya cukup homogen.
Jadi untuk tetap praktis, kami menggunakan aturan praktis ini untuk memutuskan apakah campuran itu homogen: jika properti yang diminati campuran adalah sama terlepas dari sampel yang diambil untuk pemeriksaan yang digunakan, campuran tersebut homogen.

