Perbedaan antara keadaan cair dan keadaan gas
- 1884
- 362
- Mr. Miguel Schultz
Apa pun yang ada secara fisik dan memiliki massa didefinisikan sebagai materi. Misalnya botol air Anda penting dan begitu juga air di dalamnya. Namun, kemalasan yang Anda rasakan di pagi hari atau pikiran yang Anda miliki dalam pikiran Anda tidak masalah karena mereka tidak ada secara fisik atau tidak memiliki massa. Sekarang kita tahu apa masalahnya, kita dapat menambahkan ini dengan mengatakan bahwa ada empat negara bagian di mana ada masalah. Ini adalah keadaan plasma, padat, cair dan gas. Tiga yang terakhir adalah keadaan materi dasar atau konvensional. Hampir semua yang diklasifikasikan sebagai materi dapat dikonversi menjadi salah satu dari ketiga negara bagian ini selama kondisi tertentu terpenuhi. Ini mungkin termasuk perubahan tekanan, suhu dll. Perhatikan bahwa meskipun hampir semua materi dapat dikonversi dari satu keadaan ke negara lain, pada suhu kamar dibutuhkan beberapa keadaan tertentu. Misalnya H2O adalah formula kimia untuk air yang ada dalam keadaan cair pada suhu kamar tetapi juga dapat menjadi es (keadaan padat) atau uap (keadaan gas).
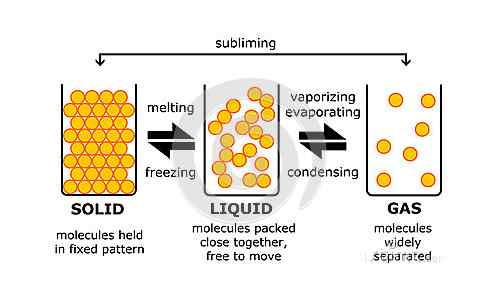
Perbedaan antara cairan dan keadaan gas adalah pada tingkat molekul, yaitu, karena karakteristik molekul yang berbeda yang terdiri dari mereka terdiri dari. Cairan apa pun terdiri dari partikel -partikel kecil yang bergetar pada atau dekat dengan posisi semula. Partikel -partikel tersebut disatukan oleh kekuatan antarmolekul. Massa cairan yang diberikan memiliki volume tetap, yaitu, wilayah tersebut ditempati tetap diperbaiki. Jika Anda menuangkan cairan dalam wadah, maka cairan akan menempati daerah yang sama dengan volumenya. Ini tidak benar untuk materi dalam keadaan gas. Partikel -partikel kecil yang membentuk gas apa pun bebas untuk bergerak. Mereka dapat bergerak di mana saja secara acak dan kekuatan daya tarik antara partikel -partikel ini sangat rendah. Mereka lebih rendah daripada gaya dalam cairan dan oleh karena itu gerakan gas disebut sebagai gerakan acak sedangkan gerakan cairan dikenal sebagai gerakan yang mengalir. Selain itu, volume gas, tidak diperbaiki tidak seperti cairan. Karena partikel -partikel itu dalam gerakan acak, mereka bebas bergerak di mana saja. Oleh karena itu, gas akan mengambil volume wadah. Ini berarti bahwa jika ada gas yang tertutup dalam wadah, ia akan memiliki volume yang sama dengan wadah. Partikel akan menyebar dan menempati daerah sebanyak yang mereka bisa. Jika jumlah gas yang sama kemudian digeser ke wadah yang lebih besar, partikel gas kemudian akan menempati volume yang lebih besar. Volume karenanya meningkat. Oleh karena itu, aman untuk mengatakan bahwa volume gas tidak diperbaiki.
Karena kekuatan tarik yang lebih lemah, partikel memiliki ruang besar di antara mereka dalam keadaan gas. Berbeda dengan ini, partikel dalam cairan memiliki ruang yang relatif lebih rendah di antara mereka. Ini juga merupakan alasan volume cairan tetap sebagai lawan dari gas.
Energi partikel adalah area lain di mana gas dan cairan berbeda. Energi partikel juga menentukan ruang di antara mereka dan karenanya keadaan materi. Partikel -partikel gas memiliki energi terbesar dari tiga keadaan dasar. Oleh karena itu, partikel menunjukkan gerakan hebat dan karenanya menyebar sebanyak yang mereka bisa. Partikel -partikel cairan, bagaimanapun, memiliki energi yang lebih rendah daripada gas. Oleh karena itu mereka biasanya tetap dekat dengan posisi awal mereka selama kondisi lainnya tetap sama.
Ringkasan perbedaan yang diungkapkan dalam poin
- Cairan terdiri dari partikel -partikel kecil yang bergetar pada atau dekat dengan posisi semula; Gas terdiri dari partikel yang bebas bergerak ke mana saja
- Gerakan gas adalah acak; Gerakan cairan disebut aliran
- Ada kekuatan molekul yang lebih kuat dari tarik -menarik dalam cairan daripada gas
- Ada jarak yang lebih besar antara partikel gas daripada cairan
- Partikel -partikel gas memiliki energi yang lebih besar daripada cairan
- Alasan yang disebutkan di atas memperhitungkan volume tetap cairan tetapi volume gas yang tidak diperbaiki dan sama dengan volume wadah di mana ia berada


