Perbedaan antara nitrat dan nitrit
- 4086
- 510
- Herbert Konopelski

Apa itu nitrat?
Ion nitrat (tidak3) adalah basa terkonjugasi dari asam nitrat. Ini terdiri dari satu nitrogen dan tiga atom oksigen. Atom nitrogen terletak di tengah dan dikelilingi oleh atom oksigen, yang secara identik terikat dalam konformasi trigonal planar. Massa molar dari anion nitrat adalah 62 g/mol. Itu terpisah dalam air untuk memberikan ion hidroksil nitrat.
Nitrat adalah senyawa kimia, garam asam nitrat. Mereka mudah larut. Nitrat digunakan dalam:
- Pertanian (pupuk mineral);
- Industri makanan (pewarna dan pengawet);
- Produksi cat, obat -obatan, plastik, kaca, bahan peledak, dll.
Nitrat ditemukan di tanah, air, dan makanan (asal tumbuhan dan hewan). Pada konsentrasi rendah (1-40 mg/m3) Mereka juga hadir di udara. Nitrat disintesis secara alami oleh bakteri nitrogen sebagai langkah perantara dalam pembentukan nitrogen. Konsentrasi alami pada tanaman dan air umumnya rendah. Kuantitas mereka di tanah subur dan air biasanya tidak melebihi 10 mg/l. Ini dapat ditingkatkan dengan menggunakan pupuk nitrogen, pengenalan kotoran ternak dan sumber lain ke dalam tanah.
Kandungan nitrat tanaman bervariasi, tergantung pada jumlahnya di tanah. Dari larutan tanah, tanaman mengekstrak nitrogen, asam amino, protein, vitamin dan zat lainnya, terutama dalam bentuk nitrat. Jika tanaman mengekstraksi lebih banyak nitrat daripada enzim nitrat reduktase dapat diproses, mereka menumpuk di dalamnya. Aktivitas nitrat reduktase tergantung pada faktor -faktor seperti cahaya, suhu dan tekanan air.
Nitrat sendiri tidak beracun. Berbahaya bagi kesehatan manusia adalah nitrit dan nitrosamin. Keduanya dapat terbentuk dari nitrat sebelum atau setelah konsumsi makanan atau air.
Nitrat memasuki tubuh manusia melalui makanan dan air minum. Makanan yang kaya nitrat adalah sayuran dan produk daging (sosis, daging asap). Apalagi yang dapat diabaikan adalah kandungan nitrat dalam produk susu dan ikan. Beberapa tanaman memiliki kemampuan untuk mengumpulkan lebih banyak nitrat. Ini adalah selada, wortel, bayam, dill, bit merah, lobak merah, zucchini, brokoli, dll.
Nitrat di udara dapat bertindak sebagai iritasi pernapasan. Studi telah menunjukkan peningkatan serangan asma yang terkait dengan peningkatan kandungan nitrat di udara.
Dosis maksimum 24 jam dosis kalium dan natrium nitrat untuk manusia adalah hingga 5 mg/kg. Keracunan terjadi pada dosis 4 g/24 jam, dosis mematikan manusia adalah 8-15 g/24 jam.
Apa itu nitrit?
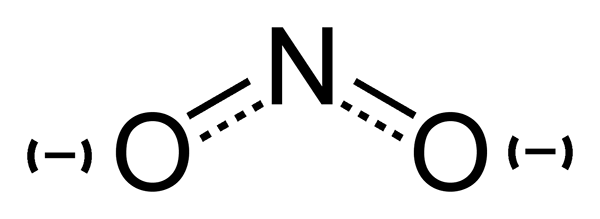
Ion nitrit (tidak2) adalah basa terkonjugasi dari asam nitrat. Anionnya simetris. Atom nitrogen terletak di tengah dan dikelilingi oleh dua atom oksigen, yang terikat secara identik. Massa molar dari anion nitrit adalah 46 g/mol.
Nitrit adalah senyawa kimia, garam atau ester dari asam nitrat. Mereka banyak digunakan dalam produksi produk daging dan ikan. Mereka memiliki aksi bakterisida. Reaksi mereka dengan mioglobin memberi daging tampilan segar dan warna merah merah muda.
Manusia dapat terpapar nitrat dalam beberapa cara. Pemupukan nitrogen yang berlebihan meningkatkan kandungan nitrat pada tanaman, dan masing -masing pada manusia (melalui makanan). Dalam tubuh manusia, nitrat dikurangi menjadi nitrit. Tanaman yang lebih tinggi juga dapat mengasimilasi nitrit dari tanah. Konversi mikrobiologis nitrat menjadi nitrit dapat terjadi ketika sayuran segar disimpan, terutama pada suhu kamar.
Nitrat, ketika dicerna, dikategorikan sebagai "mungkin karsinogenik bagi manusia". Mereka mengikat hemoglobin dalam darah dan membentuk senyawa yang disebut methemoglobin. Tidak dapat membawa oksigen ke organ dan jaringan, yang mengarah ke kondisi yang dikenal sebagai methemoglobinemia, ditandai dengan memar kulit dan selaput lendir (sianosis).
Nitrat paling berbahaya saat dikonversi menjadi nitrit sebelum tertelan. Konversi ini dapat terjadi ketika makanan disimpan secara tidak benar (suhu tinggi dan berkurangnya kandungan oksigen di dalam ruangan) atau selama memasak, terutama selama penggorengan.
Nitrit merusak struktur seluler organ dan sistem yang berbeda secara langsung, tergantung pada dosisnya. Mereka mengganggu transportasi oksigen, menyebabkan kerusakan toksik pada sistem enzim, menyebabkan perubahan mutagenik, karsinogenik, dan subseluler lainnya, mengurangi aktivitas sistem kekebalan tubuh.
Dalam keasaman rendah asam lambung, nitrit dapat dikonversi menjadi nitrosamin, yang memiliki efek karsinogenik.
Dosis nitrit maksimum yang diijinkan selama 24 jam adalah 0.2 mg/kg. Dosis mematikan manusia adalah 0.18-2.5 g/24 jam. Dipercaya bahwa mengambil 0.5 g nitrit dapat menyebabkan keracunan ringan, dan 1-2 g - hingga parah.
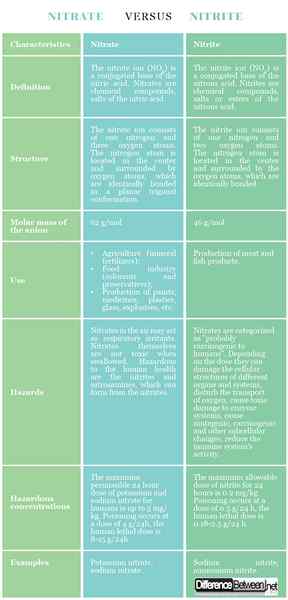
Perbedaan antara nitrat dan nitrit
-
Definisi
Nitrat: Ion nitrat (tidak3) adalah basa terkonjugasi dari asam nitrat. Nitrat adalah senyawa kimia, garam asam nitrat.
Nitrite: Ion nitrit (tidak2) adalah basa terkonjugasi dari asam nitrat. Nitrit adalah senyawa kimia, garam atau ester dari asam nitrat.
-
Struktur
Nitrat: Ion nitrat terdiri dari satu nitrogen dan tiga atom oksigen. Atom nitrogen terletak di tengah dan dikelilingi oleh atom oksigen, yang secara identik terikat dalam konformasi trigonal planar.
Nitrite: Ion nitrit terdiri dari satu nitrogen dan dua atom oksigen. Atom nitrogen terletak di tengah dan dikelilingi oleh atom oksigen, yang terikat secara identik.
-
Masa molar
Nitrat: Massa molar dari anion nitrat adalah 62 g/mol.
Nitrite: Massa molar dari anion nitrit adalah 46 g/mol.
-
Menggunakan
Nitrat: Nitrat digunakan dalam pertanian (pupuk mineral), industri makanan (pewarna dan pengawet), produksi cat, obat -obatan, plastik, kaca, bahan peledak, dll.
Nitrite: Nitrit digunakan dalam produksi produk daging dan ikan.
-
Bahaya
Nitrat: Nitrat di udara dapat bertindak sebagai iritasi pernapasan. Nitrat sendiri tidak beracun saat tertelan. Berbahaya bagi kesehatan manusia adalah nitrit dan nitrosamin, yang dapat terbentuk dari nitrat.
Nitrite: Nitrat dikategorikan sebagai "mungkin karsinogenik bagi manusia". Bergantung pada dosis mereka dapat merusak struktur seluler organ dan sistem yang berbeda, mengganggu transportasi oksigen, menyebabkan kerusakan toksik pada sistem enzim, menyebabkan perubahan mutagenik, karsinogenik dan subselular lainnya, mengurangi aktivitas sistem kekebalan tubuh kekebalan tubuh kekebalan tubuh kekebalan tubuh kekebalan.
-
Konsentrasi berbahaya
Nitrat: Dosis maksimum 24 jam dosis kalium dan natrium nitrat untuk manusia adalah hingga 5 mg/kg. Keracunan terjadi pada dosis 4 g/24 jam, dosis mematikan manusia adalah 8-15 g/24 jam.
Nitrite: Dosis nitrit maksimum yang diijinkan selama 24 jam adalah 0.2 mg/kg. Keracunan terjadi dengan dosis 0.5 g/24 jam, dosis mematikan manusia adalah 0.18-2.5 g/24 jam.
-
Contoh
Nitrat: Kalium nitrat, natrium nitrat.
Nitrite: Sodium nitrit, amonium nitrit.
Ringkasan:
- Ion nitrat (tidak3) adalah basa terkonjugasi dari asam nitrat. Nitrat adalah senyawa kimia, garam asam nitrat.
- Ion nitrit (tidak2) adalah basa terkonjugasi dari asam nitrat. Nitrit adalah senyawa kimia, garam atau ester dari asam nitrat.
- Ion nitrat terdiri dari satu nitrogen dan tiga atom oksigen. Atom nitrogen terletak di tengah dan dikelilingi oleh atom oksigen, yang secara identik terikat dalam konformasi trigonal planar. Ion nitrit terdiri dari satu nitrogen dan dua atom oksigen. Atom nitrogen terletak di tengah dan dikelilingi oleh atom oksigen, yang terikat secara identik.
- Massa molar anion nitrat adalah 62 g/mol, sedangkan massa molar dari anion nitrit adalah 46 g/mol.
- Nitrat digunakan dalam pertanian, industri makanan, produksi cat, obat -obatan, plastik, kaca, bahan peledak, dll. Nitrit digunakan dalam produksi produk daging dan ikan.
- Nitrat di udara dapat bertindak sebagai iritasi pernapasan. Nitrat sendiri tidak beracun saat tertelan. Berbahaya bagi kesehatan manusia adalah nitrit dan nitrosamin, yang dapat terbentuk dari nitrat. Nitrat dikategorikan sebagai "mungkin karsinogenik bagi manusia". Bergantung pada dosis mereka dapat merusak struktur seluler organ dan sistem yang berbeda, mengganggu transportasi oksigen, menyebabkan kerusakan toksik pada sistem enzim, menyebabkan perubahan mutagenik, karsinogenik dan subselular lainnya, mengurangi aktivitas sistem kekebalan tubuh kekebalan tubuh kekebalan tubuh kekebalan tubuh kekebalan.
- Dosis maksimum 24 jam dosis kalium dan natrium nitrat untuk manusia adalah hingga 5 mg/kg. Keracunan terjadi pada dosis 4 g/24 jam, dosis mematikan adalah 8-15 g/24 jam. Dosis nitrit maksimum yang diijinkan selama 24 jam adalah 0.2 mg/kg. Keracunan terjadi dengan dosis 0.5 g/24 jam, dosis mematikan adalah 0.18-2.5 g/24 jam.

