Perbedaan antara CIS dan Trans

- 3362
- 141
- Isaac Veum DDS
Isomerisme CIS-Trans terdiri dari kemungkinan menempatkan kelompok substituen pada satu atau pada sisi yang berbeda dari bidang ikatan rangkap atau siklus non-aromatik. Isomer cis-trans milik diastereomer karena mereka bukan cermin satu sama lain. Isomer CIS dan trans ditemukan di antara senyawa organik dan anorganik.
Nomenklatur CIS-Trans menggambarkan posisi relatif pengganti, dan tidak memberikan deskripsi stereokimia, sebagai E, Z- nomenklatur, hanya berlaku untuk alkena.
Keberadaan cis dan isomer trans yang terpisah hanya dimungkinkan karena penghalang energi rotasi yang tinggi di sekitar ikatan rangkap.

Apa itu cis?
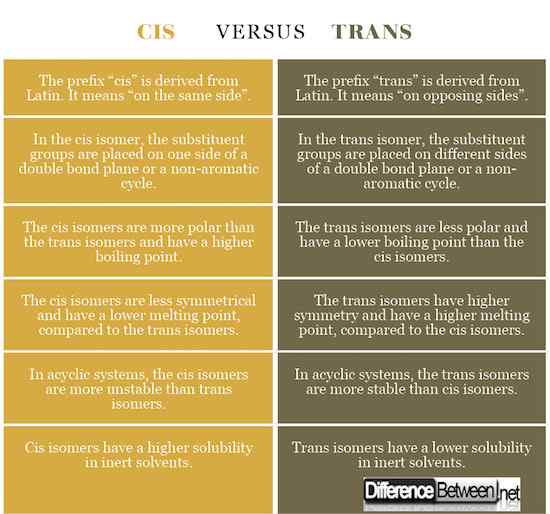
Awalan "CIS" berasal dari bahasa Latin. Itu berarti "di sisi yang sama". Di isomer cis, kelompok substituen ditempatkan di satu sisi bidang ikatan rangkap atau siklus non-aromatik.
CIS dan isomer trans berbeda dalam sifat fisiknya, karena ketidaksetaraan pada momen dipol secara keseluruhan dan bentuk molekul.
Titik didih relatif ditentukan oleh polaritas. Itu menyebabkan peningkatan gaya antarmolekul, yang menghasilkan peningkatan titik didih. Isomer cis, yang lebih kutub dari isomer trans, memiliki titik didih yang lebih tinggi. Perbedaannya bisa kecil, seperti misalnya di alkena dengan rantai lurus. Perbedaan yang lebih besar diamati pada zat dengan ikatan kutub. Contoh untuk zat seperti itu adalah 1,2-dikloroetene. Titik didih dari isomer cisnya adalah 60.3 ° C, dan dari isomer trans - dengan 12.8 ° C lebih rendah. Alasan perbedaannya adalah bahwa dalam cis isomer dua momen dipol ikatan polar C-Cl pasangan dan menghasilkan dipol molekuler secara keseluruhan. Akibatnya terjadi gaya dipol-dipol antarmolekul, yang menaikkan titik didih.
Simetri memungkinkan pengemasan zat padat yang lebih baik. Sebagai hasil dari simetri yang berbeda dari molekul, cis dan isomer trans berbeda dalam titik lelehnya. Isomer cis, yang kurang simetris, memiliki titik leleh yang lebih rendah, dibandingkan dengan isomer trans.
Fitur lain dari isomer cis adalah bahwa mereka memiliki kepadatan yang lebih tinggi daripada rekan trans mereka.
Biasanya, dalam sistem asiklik, isomer cis lebih tidak stabil daripada isomer trans. Alasan untuk ini adalah peningkatan interaksi sterik yang tidak menguntungkan dari substituen dalam isomer cis. Secara umum, isomer cis memiliki kelarutan yang lebih tinggi dalam pelarut inert.
Apa itu trans?
Awalan "trans" berasal dari bahasa Latin. Itu berarti "di sisi lawan". Dalam isomer trans, kelompok substituen ditempatkan di sisi berbeda dari bidang ikatan rangkap atau siklus non-aromatik.
Titik didih dari isomer trans lebih rendah dari pada isomer cis. Perbedaannya lebih signifikan pada zat dengan ikatan kutub. Dalam isomer trans 1,2-dikloroetena, dua momen ikatan C-CL saling membatalkan dan molekul memiliki dipol nol bersih. Akibatnya, tidak ada gaya dipol-dipol antarmolekul, yang mengurangi titik didih.
Simetri molekul adalah kunci dalam penentuan titik leleh, karena pengemasan zat padat yang lebih baik. Contohnya adalah asam oleat (isomer cis) dan asam elaidic (trans isomer). Titik lebur isomer cis adalah 13.4 ° C, isomer trans meleleh pada 43 ° C. Alasan untuk ini adalah bahwa isomer trans lebih lurus, berkemas lebih baik, dan karenanya - memiliki titik leleh yang jauh lebih tinggi.
Isomer trans memiliki kepadatan yang lebih rendah dari rekan CIS mereka. Dalam sistem asiklik, isomer trans lebih stabil daripada isomer cis. Secara umum, isomer cis memiliki kelarutan yang lebih tinggi dalam pelarut inert.
Perbedaan antara CIS dan Trans
-
Definisi CIS dan Trans
Cis: Awalan "CIS" berasal dari bahasa Latin. Itu berarti "di sisi yang sama". Di isomer cis, kelompok substituen ditempatkan di satu sisi bidang ikatan rangkap atau siklus non-aromatik.
Trans: Awalan "trans" berasal dari bahasa Latin. Itu berarti "di sisi lawan". Dalam isomer trans, kelompok substituen ditempatkan di sisi berbeda dari bidang ikatan rangkap atau siklus non-aromatik.
-
Polaritas dan titik didih CIS dan trans
Cis: Polaritas menyebabkan peningkatan gaya antarmolekul, yang mengakibatkan peningkatan titik didih. Isomer cis, yang lebih kutub dari isomer trans, memiliki titik didih yang lebih tinggi.
Trans: Isomer trans kurang polar dan memiliki titik didih yang lebih rendah daripada isomer cis. Perbedaannya lebih signifikan pada zat dengan ikatan kutub.
-
Simetri dan titik leleh CIS dan trans
Cis: Isomer cis kurang simetris dan memiliki titik leleh yang lebih rendah, dibandingkan dengan isomer trans.
Trans: Isomer trans memiliki simetri yang lebih tinggi dan titik leleh yang lebih tinggi, dibandingkan dengan isomer cis.
-
Stabilitas dan kelarutan CIS dan trans
Cis: Dalam sistem asiklik, isomer cis lebih tidak stabil daripada isomer trans. Mereka memiliki kelarutan yang lebih tinggi dalam pelarut inert.
Trans: Dalam sistem asiklik, isomer trans lebih stabil daripada isomer cis. Mereka memiliki kelarutan yang lebih rendah dalam pelarut inert.
Ringkasan Cis vs. Trans:
- Isomerisme CIS-Trans terdiri dari kemungkinan menempatkan kelompok substituen pada satu atau pada sisi yang berbeda dari bidang ikatan rangkap atau siklus non-aromatik.
- Keberadaan cis dan isomer trans yang terpisah hanya dimungkinkan karena penghalang energi rotasi yang tinggi di sekitar ikatan rangkap. Mereka ditemukan baik di antara senyawa organik dan anorganik.
- Awalan “CIS” dan trans berasal dari bahasa Latin. Cis berarti "di sisi yang sama", trans berarti "di sisi lawan".
- Dalam isomer cis, gugus substituen ditempatkan di satu sisi, sedangkan dalam isomer trans, gugus substituen ditempatkan pada sisi yang berbeda dari bidang ikatan rangkap atau siklus non-aromatik.
- Polaritas menyebabkan peningkatan kekuatan antar molekul, yang menghasilkan peningkatan titik didih. Isomer cis lebih polar daripada isomer trans dan memiliki titik didih yang lebih tinggi. Perbedaannya lebih signifikan pada zat dengan ikatan kutub.
- Isomer cis kurang simetris dan memiliki titik leleh yang lebih rendah, dibandingkan dengan isomer trans.
- Dalam sistem asiklik, isomer cis lebih tidak stabil daripada isomer trans. Mereka memiliki kelarutan yang lebih tinggi dalam pelarut inert.
- « Perbedaan antara Samsung Galaxy S7 dan Galaxy S7 Edge
- Perbedaan antara endosmosis dan eksosmosis »