Perbedaan antara energi ikatan dan entalpi energi disosiasi ikatan
- 1592
- 332
- Herbert Konopelski
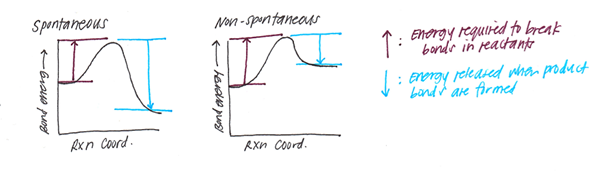
Energi Bond vs. Energi disosiasi ikatan (entalpi)
Energi ikatan adalah nilai rata-rata energi disosiasi ikatan gas-fase (biasanya pada suhu 298 K) yang ada di antara jenis atom yang sama. Namun, energi ikatan dan energi disosiasi ikatan tidak sama. Ikatan Disosiasi Energi adalah perubahan entalpi standar ketika ikatan kovalen (juga disebut sebagai ikatan molekuler, adalah ikatan kimia antara dua atom non-logam, yang melibatkan pembagian pasangan elektron antara atom-atom tersebut) dibelah oleh homolisis (kerusakan dengan yang sama potongan) untuk memberikan fragmen; yang biasanya merupakan spesies radikal. Oleh karena itu, perbedaan utama antara energi ikatan dan energi disosiasi ikatan adalah bahwa energi ikatan adalah nilai rata -rata sedangkan energi disosiasi ikatan adalah nilai tertentu untuk ikatan tertentu.
Apa itu energi ikatan dan energi disosiasi ikatan (entalpi)?
Energi ikatan
Energi ikatan mengacu pada energi yang diperlukan untuk memecah semua ikatan yang ada antara 2 jenis spesies kimia yang sama dalam suatu senyawa.
Plot energi potensial dari sistem atom 2 dan jarak antara spesies kimia menunjukkan jarak di mana energi terlalu sedikit. Jarak ini terungkap adalah panjang ikatan antara atom.
Semakin tinggi energi ikatan (E) yang dikaitkan dengan pasangan spesies kimia tertentu, semakin kuat ikatan tersebut dikatakan, dan lebih rendah jarak antara 2 atom.
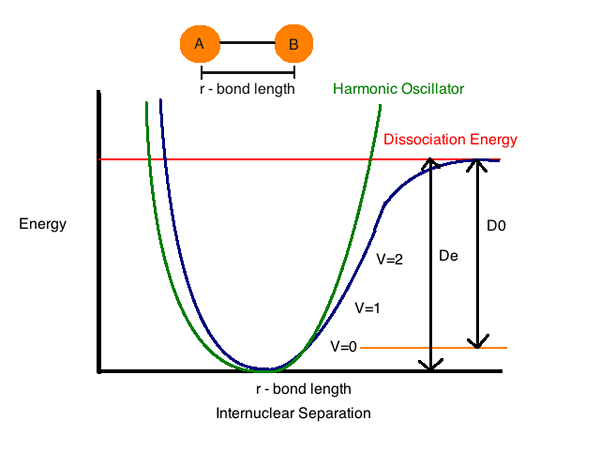
Energi disosiasi ikatan
Energi Disosiasi Obligasi (Enthalpy) (H) adalah jumlah energi yang dibutuhkan untuk memecah ikatan tertentu dalam homolisis. Kita dapat mendefinisikannya sebagai perubahan entalpi yang terjadi ketika ikatan mengalami pembelahan dengan homolisis. Energi disosiasi ikatan khusus untuk satu ikatan.
Entalpi ikatan, (sifat termodinamika dari suatu sistem) atau energi disosiasi ikatan, disebut sebagai perubahan entalpi standar ketika ikatan dibelah (dipisahkan atau dibagi) oleh homolise (dipecah menjadi potongan -potongan kecil) dengan reaktan dan produk reaksi homolisis pada pada reaksi pada pada reaksi pada pada reaksi pada pada reaksi homolisis pada saat homolisis di 0 K (Absolute Zero).
Perbedaan antara energi ikatan & energi disosiasi ikatan (entalpi)
Keterangan
Energi ikatan
Energi ikatan juga disebut sebagai entalpi ikatan dan didefinisikan sebagai ukuran kekuatan ikatan dalam ikatan kimia. Energi obligasi adalah nilai rata -rata
Energi disosiasi ikatan
Energi disosiasi ikatan didefinisikan sebagai perubahan entalpi standar yang diperlukan untuk memecahkan ikatan kimia
Produk
Energi ikatan
Energi ikatan menawarkan energi yang dibutuhkan untuk membentuk atom yang merupakan bahan awal untuk pembentukan ikatan.
Energi disosiasi ikatan
Energi disosiasi ikatan menyediakan energi yang dibutuhkan untuk membentuk radikal bebas dari atom yang menciptakan ikatan tertentu itu.
Contoh
Energi ikatan
Dalam kimia, energi ikatan (E) atau entalpi ikatan (H) adalah ukuran kekuatan ikatan dalam ikatan kimia.... misalnya, energi ikatan karbon-hidrogen (C-H) dalam metana (CH4) adalah perubahan entalpi yang terlibat dengan memecah satu molekul CH4 menjadi atom karbon (C) dan empat radikal hidrogen (H), dibagi dengan empat.
Energi disosiasi ikatan
Misalnya, dalam molekul metana, energi disosiasi ikatan untuk ikatan C-H adalah 439 kJ/mol, 460 kJ/mol, 423 kJ/mol dan 339 kJ/mol. Namun, energi ikatan C-H metana adalah 414 kJ/mol, yang merupakan rata-rata dari keempat nilai. Lebih lanjut, untuk molekul, energi disosiasi ikatan mungkin tidak selalu sama dengan energi ikatan (seperti untuk contoh metana yang diberikan di atas). Untuk molekul diatomik, energi ikatan dan energi disosiasi ikatan adalah sama.
Simbol
Energi ikatan
Itu dilambangkan dengan e
Energi disosiasi ikatan
Itu dilambangkan dengan h
Pembentukan ikatan
Energi ikatan
Ini memberikan energi yang dibutuhkan untuk membentuk atom yang merupakan bahan awal untuk pembentukan ikatan
Energi disosiasi ikatan
Ini memberikan energi yang diperlukan untuk membuat radikal bebas dari atom yang menciptakan ikatan tertentu
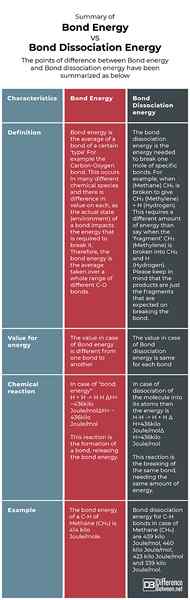
Ringkasan Energi Bond VS. Energi disosiasi ikatan
Titik perbedaan antara energi ikatan dan energi disosiasi ikatan telah dirangkum seperti di bawah ini:
- « Perbedaan antara yurisdiksi materi pelajaran dan yurisdiksi pribadi
- Perbedaan antara perubahan iklim dan penipisan ozon »

